
보이지 않지만 모든 것을 결정하는 숫자
폐수처리 현장에서 가장 먼저 측정하는 것은 무엇일까요? BOD도, COD도, SS도 아닙니다. 바로 pH입니다.
pH는 단순한 숫자가 아닙니다. 이 작은 수치 하나가 미생물의 생사, 화학 반응의 성패, 설비의 수명, 방류수 기준의 충족 여부를 결정합니다. pH 관리에 실패하면 아무리 좋은 설비와 약품을 사용해도 폐수처리는 실패합니다.
이 글에서는 pH가 왜 폐수처리의 절대 핵심인지, 그리고 어떻게 하면 pH를 안정적이고 효율적으로 관리할 수 있는지 과학적 원리부터 실무 노하우까지 상세히 살펴보겠습니다.
1. pH란 무엇인가? - 기초부터 확실하게
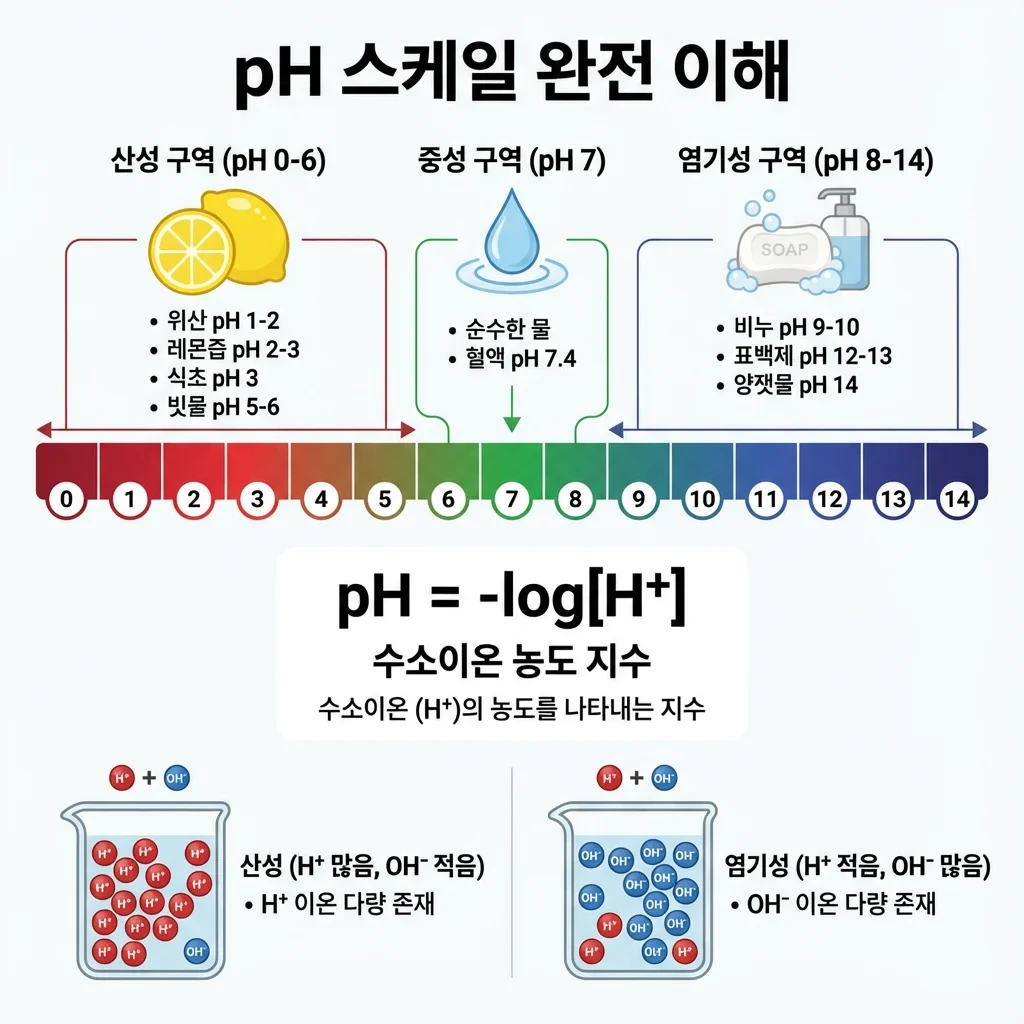
1) pH의 정의
pH (potential of Hydrogen) = 수소 이온 농도 지수
화학적 정의:
pH = -log₁₀[H⁺]
여기서 [H⁺]는 수소 이온(H⁺)의 몰 농도입니다.
2) pH 스케일 (0~14)
> 산성 구역 (pH 0~6)
- H⁺ 많음, OH⁻ 적음
- 실생활 예시:
- pH 1~2: 위산, 염산
- pH 2~3: 레몬즙, 식초
- pH 3~4: 오렌지주스, 사과
- pH 5~6: 빗물, 커피
> 중성 구역 (pH 7)
- H⁺ = OH⁻ (균형)
- 실생활 예시:
- pH 7.0: 순수한 물
- pH 7.4: 사람의 혈액
> 염기성(알칼리성) 구역 (pH 8~14)
- H⁺ 적음, OH⁻ 많음
- 실생활 예시:
- pH 8~9: 해수, 베이킹소다
- pH 9~10: 비누, 치약
- pH 11~12: 암모니아수
- pH 12~13: 표백제
- pH 14: 양잿물(수산화나트륨)
3) pH의 로그 스케일 특성
중요: pH는 로그 스케일이므로 pH 1 차이 = 10배 차이
예시:
- pH 3 → pH 4: 산성도 1/10로 감소
- pH 5 → pH 3: 산성도 100배 증가
- pH 7 → pH 10: 알칼리성 1,000배 증가
따라서 pH 1~2의 변동도 매우 큰 영향을 미칩니다.
2. pH가 폐수처리에 미치는 5가지 결정적 영향
2-1. 영향 1: 생물학적 처리 효율 (가장 중요)

생물학적 폐수처리는 미생물의 대사 활동에 전적으로 의존합니다. 그런데 미생물은 pH에 극도로 민감합니다.
최적 pH 범위: 6.5~7.5
이 범위에서만:
- 미생물 활성 100%
- BOD 제거율 95% 이상
- 질산화 반응 정상 작동
- 인 제거 효율 최대
pH 이탈 시 영향
pH 3 이하 (극산성):
- ❌ 미생물 즉시 사멸
- ❌ 효소 단백질 변성
- ❌ 생물학적 처리 완전 정지
- 결과: 폐수처리 불가능
pH 4~5 (산성):
- ⚠️ 미생물 활성 30% 저하
- ⚠️ 질산화 박테리아 활동 중단
- ⚠️ BOD 제거율 70% 이하
- 결과: 방류수 기준 초과 위험
pH 8~9 (약알칼리):
- ⚠️ 미생물 활성 40% 저하
- ⚠️ 암모니아(NH₃) 독성 증가
- ⚠️ 인 제거 효율 감소
- 결과: 수질 불안정
pH 10 이상 (강알칼리):
- ❌ 세포막 파괴
- ❌ 미생물 사멸
- ❌ 생물학적 처리 정지
- 결과: 폐수처리 불가능
핵심 메시지: pH 6.5~7.5 범위를 ±0.3 이내로 유지해야 안정적인 처리 가능
2-2. 영향 2: 화학적 침전 반응
pH는 중금속과 인의 침전 제거 효율을 결정합니다.
> 중금속 수산화물 침전
Cu²⁺ + 2OH⁻ → Cu(OH)₂↓ (pH 8~9에서 최적)
Pb²⁺ + 2OH⁻ → Pb(OH)₂↓ (pH 9~10에서 최적)
Zn²⁺ + 2OH⁻ → Zn(OH)₂↓ (pH 8~9에서 최적)
pH가 낮으면 (산성):
- 수산화물 침전 형성 안 됨
- 중금속이 수용액 상태로 방류
- 방류수 기준 초과
pH가 너무 높으면 (강알칼리):
- 양쪽성 수산화물이 다시 용해 (재용출)
- 예: Zn(OH)₂ + 2OH⁻ → Zn(OH)₄²⁻ (가용성)
> 인 제거 반응
Ca²⁺ + PO₄³⁻ → Ca₃(PO₄)₂↓ (pH 8~9.5에서 최적)
pH 7 이하: 인산 침전 형성 어려움 pH 9.5 이상: 과량의 슬러지 발생
2-3. 영향 3: 독성 물질의 활성
pH는 암모니아(NH₃)의 독성을 크게 좌우합니다.
암모니아 평형 반응
NH₄⁺ (무독성) ⇌ NH₃ (독성) + H⁺
pH 7 이하: NH₄⁺ 형태 (무독성) pH 9 이상: NH₃ 형태 (독성) 급증
pH 9.5에서: 암모니아 독성이 pH 7 대비 100배 이상 증가
2-4. 영향 4: 설비 부식 및 손상
> 산성 폐수 (pH < 5)
- 금속 배관 부식
- 콘크리트 조 용해
- 펌프·교반기 수명 단축
- 수리비용 연간 수천만 원 추가
> 알칼리성 폐수 (pH > 9)
- 비금속 재질 손상
- 고무·플라스틱 씰 열화
- 센서 오작동
최적 pH 범위 (6~8): 설비 수명 2~3배 연장
2-5. 영향 5: 약품 효율
응집제(PAC, 황산반토 등)의 효율은 pH에 절대적으로 의존합니다.
PAC (Poly Aluminum Chloride)
최적 pH 범위: 6.5~7.5
- pH 5 이하: 응집 효율 50% 이하
- pH 9 이상: 응집 효율 30% 이하
pH 관리 실패 시: 약품비 2~3배 증가 + 수질 악화
3. 국내 방류수 pH 기준과 법적 책임
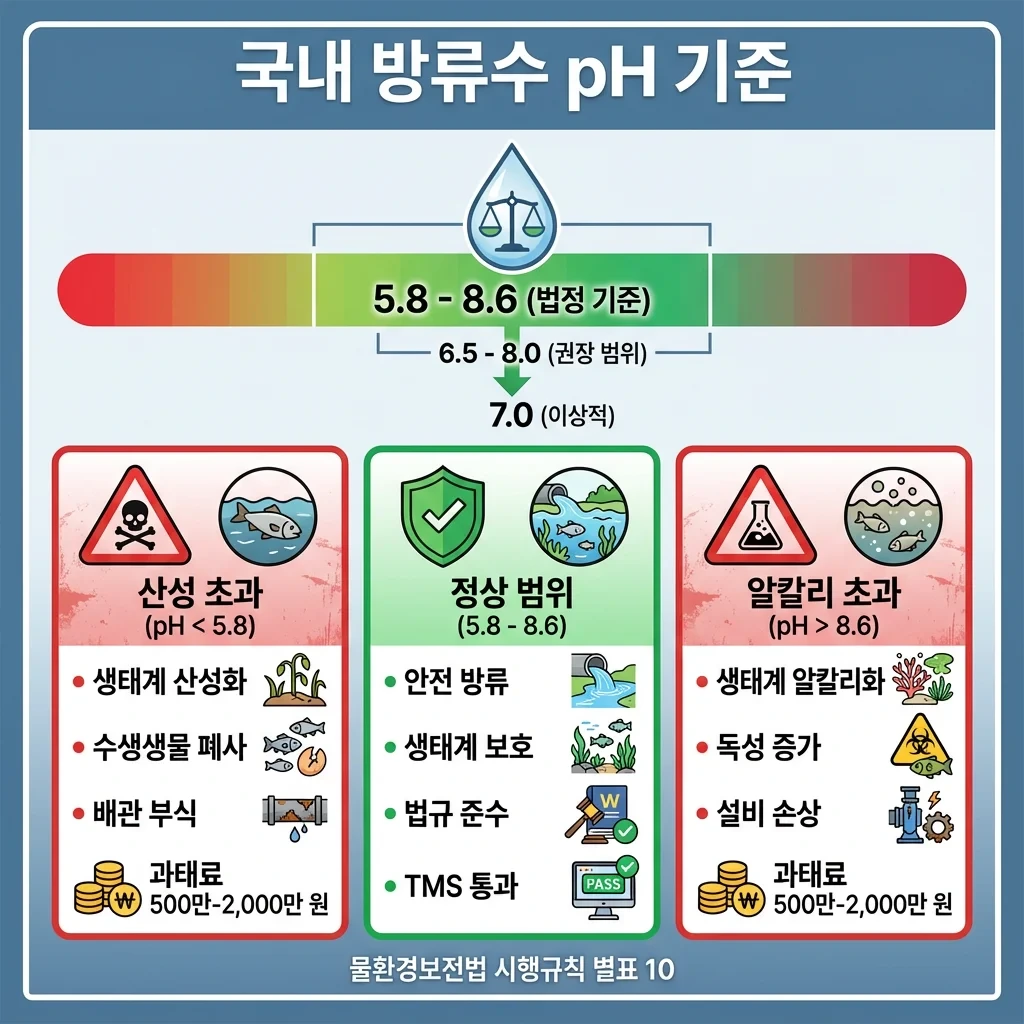
1) 법정 pH 기준
물환경보전법 시행규칙 별표 10
공공폐수처리시설 방류수 기준
- 법정 범위: pH 5.8~8.6
- 권장 범위: pH 6.5~8.0
- 이상적: pH 7.0
산업폐수 배출허용기준
- 업종에 따라 동일 또는 더 엄격
- 특정 업종(반도체, 전자부품): pH 6.0~8.5
2) 위반 시 법적 제재
> 산성 초과 (pH < 5.8)
환경적 피해:
- 하천·호수 산성화
- 수생생물 폐사 (어류 아가미 손상)
- 생태계 교란
시설 피해:
- 방류 배관 부식
- 하수관거 손상
법적 제재:
- 1차 위반: 과태료 500만 원
- 2차 위반: 과태료 1,000만 원
- 3차 위반: 과태료 2,000만 원
- 반복 위반: 조업정지 명령 가능
> 정상 범위 (pH 5.8~8.6)
결과:
- ✅ 안전 방류
- ✅ 생태계 보호
- ✅ 법규 준수
- ✅ TMS 통과
- ✅ 기업 신뢰도 유지
> 알칼리 초과 (pH > 8.6)
환경적 피해:
- 하천·호수 알칼리화
- 암모니아 독성 증가
- 조류(algae) 대번식
시설 피해:
- 비금속 설비 손상
- 생물학적 처리 교란
법적 제재:
- 산성 초과와 동일한 과태료 체계
TMS(수질원격감시체계) 실시간 감시
2008년부터 의무화:
- pH를 포함한 수질 항목 24시간 실시간 측정
- 환경부 중앙 서버로 자동 전송
- 이상 수치 즉시 감지 → 현장 점검
조작 불가:
- 센서 교정 이력 자동 기록
- 데이터 조작 시 형사 처벌 (징역형 가능)
4. pH 중화 화학 반응의 원리
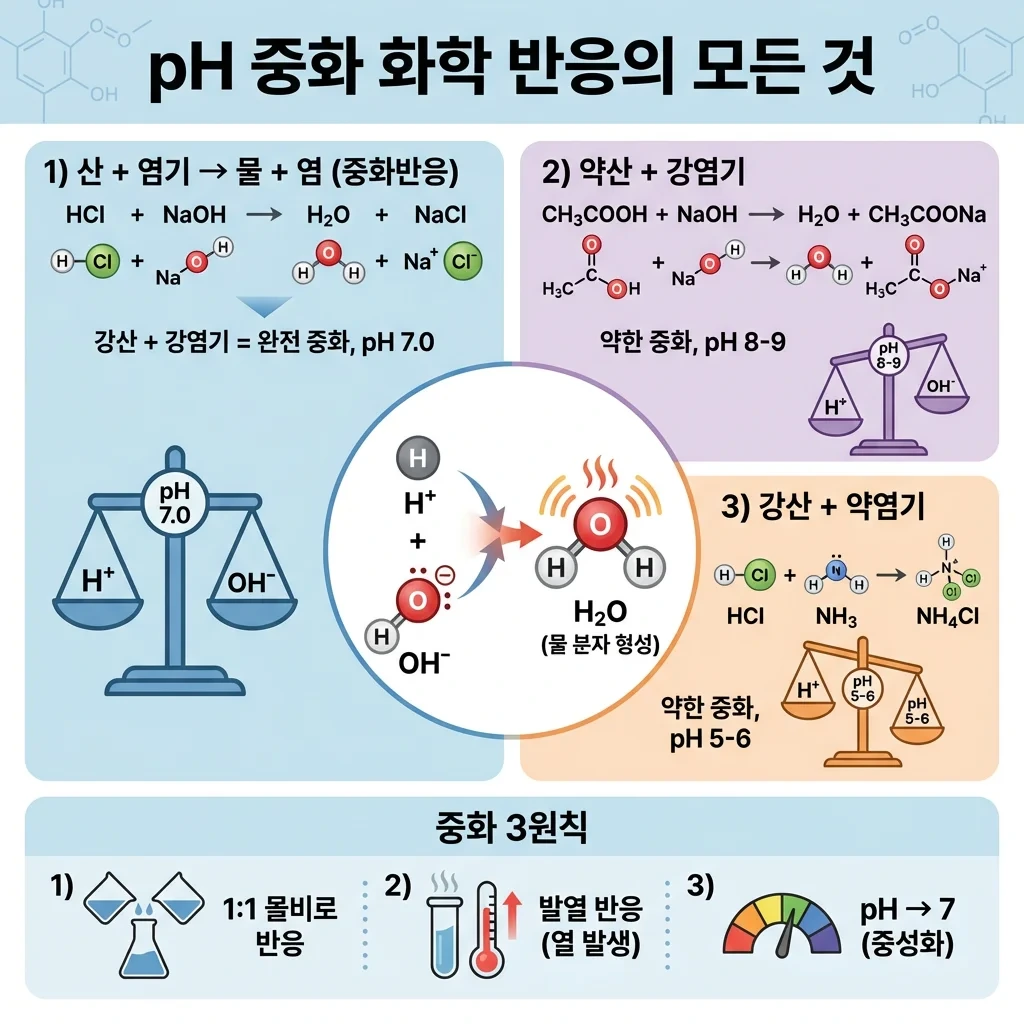
중화 반응의 기본 원리
중화 반응: 산과 염기가 만나 물과 염을 생성하는 반응
산 + 염기 → 물 + 염
핵심 반응:
H⁺ + OH⁻ → H₂O
3가지 중화 반응 유형
1) 강산 + 강염기 = 완전 중화 (pH 7.0)
HCl + NaOH → H₂O + NaCl
(염산) (수산화나트륨) (물) (소금)
특징:
- 1:1 몰비로 완전 반응
- 최종 pH: 7.0 (정확한 중성)
- 발열 반응 (열 발생)
실무 적용:
- 산성 폐수를 NaOH로 중화
- 알칼리 폐수를 HCl로 중화
2) 약산 + 강염기 = 약한 중화 (pH 8~9)
CH₃COOH + NaOH → H₂O + CH₃COONa
(아세트산) (수산화나트륨) (물) (아세트산나트륨)
특징:
- 반응 후 pH 8~9 (약알칼리)
- 아세트산염이 완충 작용
3) 강산 + 약염기 = 약한 중화 (pH 5~6)
HCl + NH₃ → NH₄Cl
(염산) (암모니아) (염화암모늄)
특징:
- 반응 후 pH 5~6 (약산성)
- 암모늄염이 완충 작용
중화 반응 3원칙
원칙 1: 1:1 몰비 반응
- 산의 H⁺ 1몰과 염기의 OH⁻ 1몰이 반응
- 과량 투입 시 pH 과도 상승 또는 하강
원칙 2: 발열 반응
- 중화 반응은 에너지 방출 (발열)
- 대량 폐수 처리 시 온도 10~20°C 상승 가능
- 냉각 시스템 필요
원칙 3: pH → 7 (중성화)
- 목표: 최종 pH 7.0 ± 0.5
- 실무에서는 6.5~7.5 범위 유지
5. 기존 방식 vs RSWT: pH 관리의 혁신

기존 소석회 방식의 문제점
문제 1: Over-neutralization (과도한 알칼리화)
소석회 투입 시:
Ca(OH)₂ + 2H⁺ → Ca²⁺ + 2H₂O
pH 변화:
- 유입: pH 2~4 (강산성)
- 소석회 투입 후: pH 10~12 (강알칼리) ← 문제!
- 산 재투입 후: pH 7 (중성)
왜 문제인가?
- pH 10~12에서 미생물 일시 사멸
- 암모니아 독성 급증
- 설비 부식
- 산(HCl) 재투입 비용 연간 수천만 원
문제 2: pH 변동폭이 큼
- pH 변동폭: ±2.0 이상
- 안정적인 생물학적 처리 불가능
- 방류수 수질 불안정
문제 3: 2단계 공정 필요
1단계: 소석회로 과도하게 중화 2단계: 산(HCl)로 pH 재조정
→ 약품비 2배, 운영 복잡도 증가, 설비 2배
RSWT 완충 시스템의 혁신
장점 1: Auto-neutralization (자동 중화)
RSWT 투입 시:
CaCO₃ + 2H⁺ → Ca²⁺ + H₂O + CO₂↑
pH 변화:
- 유입: pH 2~4 (강산성)
- RSWT 투입 후: pH 6.5~7.5 (중성) ← 완벽!
- 추가 약품 불필요
왜 완벽한가?
- pH가 자연스럽게 6.5~7.5에 수렴
- 과도한 알칼리화 없음
- 미생물에 무해
장점 2: pH 변동폭이 작음
- pH 변동폭: ±0.3 이내
- 안정적인 생물학적 처리 가능
- 방류수 수질 일정
장점 3: 1단계 공정
RSWT 투입 → pH 자동 중화 완료
→ 약품비 50% 절감, 운영 간소화, 설비 절반
pH 변화 곡선 비교
소석회 방식:
pH 2 → (급상승) → pH 12 → (급하강) → pH 7
- 그래프: 뾰족한 스파이크 형태
- 변동 심함
RSWT 방식:
pH 2 → (완만 상승) → pH 7
- 그래프: 부드러운 곡선 형태
- 변동 최소
6. RSWT 패각의 완충 작용 메커니즘 (과학적 해설)
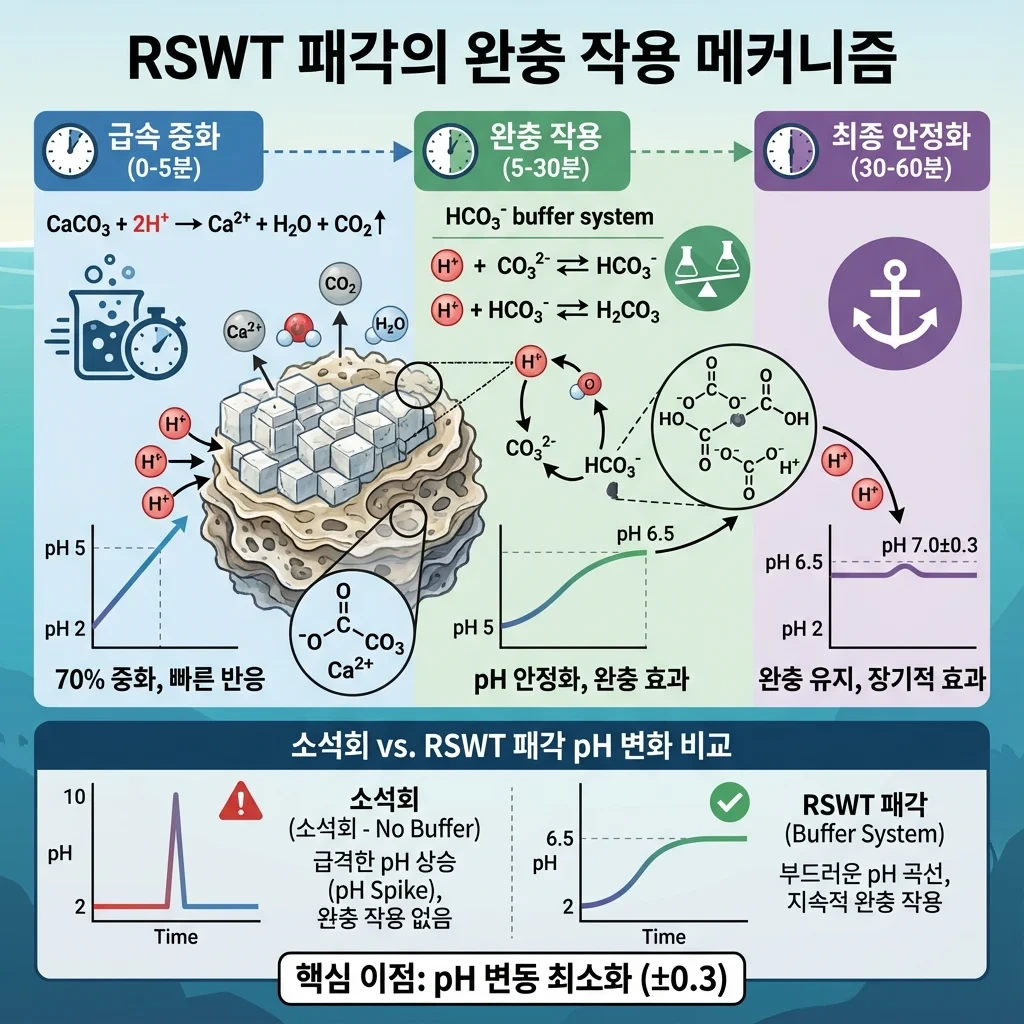
3단계 완충 시스템
> Stage 1: 급속 중화 (0~5분)
화학 반응:
CaCO₃ + 2H⁺ → Ca²⁺ + H₂O + CO₂↑
진행 상황:
- pH 2 → 5
- 중화율 70%
- 반응 속도: 매우 빠름
메커니즘:
- 패각 표면의 CaCO₃가 H⁺와 직접 반응
- CO₂ 기체 방출로 반응 촉진
> Stage 2: 완충 작용 (5~30분)
화학 반응:
CO₂ + H₂O ⇌ H₂CO₃ (탄산)
H₂CO₃ ⇌ H⁺ + HCO₃⁻ (탄산수소이온)
HCO₃⁻ ⇌ H⁺ + CO₃²⁻ (탄산이온)
진행 상황:
- pH 5 → 6.5
- 안정화 진행
- 반응 속도: 중간
메커니즘:
- 탄산-탄산수소 완충계 형성
- H⁺가 증가하면 HCO₃⁻가 흡수
- H⁺가 감소하면 HCO₃⁻가 방출
- pH를 6.5 근처에 유지
> Stage 3: 최종 안정화 (30~60분)
진행 상황:
- pH 6.5 → 7.0 ± 0.3
- 완충 유지
- 반응 속도: 느림
메커니즘:
- 완충계가 계속 작동하여 pH 변동 최소화
- 외부 교란에도 pH 안정 유지
소석회 vs RSWT 비교
항목 소석회 RSWT
| 완충 시스템 | ❌ 없음 | ✅ 탄산-탄산수소 완충계 |
| pH 곡선 | 급상승 스파이크 | 완만한 곡선 |
| 최종 pH | 10~12 → 7 (2단계) | 6.5~7.5 (1단계) |
| pH 변동폭 | ±2.0 | ±0.3 |
| 추가 약품 | 필요 (HCl) | 불필요 |
핵심 차이: RSWT는 완충 시스템이 내장되어 pH를 자동으로 안정화
7. pH 관리 5대 핵심 원칙 (실무 가이드)

원칙 1: 실시간 모니터링
설비:
- pH 센서 설치: 유입조, 반응조, 방류조 각 1개 이상
- 정밀도: ±0.1 pH
- 교정 주기: 월 1회 (표준 완충액 사용)
시스템:
- 24시간 데이터 로깅: 분 단위 기록
- 이상 알람 설정: pH < 6.0 또는 pH > 8.5 시 즉시 알림
- 원격 모니터링: 모바일/PC로 실시간 확인
효과:
- 이상 징후 조기 발견
- 대응 시간 단축 (30분 → 5분)
- 법규 위반 예방
원칙 2: 완충 시스템 도입
RSWT 등 완충제 사용:
- 급격한 pH 변동 방지
- 안정적인 중화
- 미생물 보호
효과:
- pH 변동폭 ±2.0 → ±0.3
- 생물학적 처리 효율 20% 향상
- 약품비 30~40% 절감
원칙 3: 2단계 검증
온라인 센서 측정:
- 실시간 pH 모니터링
- 자동 기록
실험실 분석 (매일):
- 휴대용 pH 미터로 교차 검증
- 센서 오차 확인
- 정확도 확보
센서 교정:
- 월 1회 정기 교정
- 표준 완충액 (pH 4.0, 7.0, 10.0) 사용
- 교정 이력 기록 보관
원칙 4: 사전 예방
유입수 pH 패턴 분석:
- 시간대별, 요일별 pH 변동 데이터 축적
- 패턴 인식으로 이상 예측
급변 시 대응 매뉴얼:
- pH < 5.5: RSWT 투입량 20% 증가
- pH > 8.0: 산 투입 또는 유입 일시 차단
- 비상 연락망 24시간 운영
비상 약품 재고:
- RSWT 등 중화제: 3일분 상시 확보
- 산·알칼리 조정제: 7일분 확보
원칙 5: 법규 준수
방류수 기준 (5.8~8.6):
- 목표 범위: 6.5~8.0 (안전 마진)
- 이상적 pH: 7.0
TMS 실시간 전송:
- 환경부 서버로 자동 전송
- 데이터 조작 엄격 금지
기록 보관 (3년):
- pH 측정 데이터 3년간 보관 의무
- 센서 교정 이력 문서화
- 감사 대비 체계적 관리
8. pH 관리 실패 사례와 교훈
사례 1: 소석회 과량 투입으로 미생물 전멸
배경: 중형 식품 공장 문제: 소석회 자동 투입 밸브 고장 결과:
- pH 2 → 13 급상승
- 활성슬러지 미생물 전멸
- 생물학적 처리 3주간 중단
- 손실액: 약 1.2억 원 (폐수 위탁처리 + 미생물 재배양)
교훈:
- pH 상한 알람 필수 (pH > 9.0)
- 자동 밸브 이중 안전장치
- RSWT 같은 완충제 사용 시 이런 사고 예방 가능
사례 2: pH 센서 오작동으로 방류수 기준 초과
배경: 소형 도금 공장 문제: pH 센서 교정 미실시 (6개월간) 결과:
- 실제 pH 9.2를 센서가 pH 7.5로 오판
- 방류수 기준 초과 (5.8~8.6)
- 과태료: 1,000만 원
- 공장 평판 손상
교훈:
- 월 1회 센서 교정 필수
- 실험실 분석으로 교차 검증
- TMS 데이터 주기적 확인
사례 3: 유입수 급변에 대응 실패
배경: 대형 염색 공장 문제: 공정 변경으로 유입 폐수 pH 2 → 5로 급변 결과:
- 기존 RSWT 투입량 부족
- 반응조 pH 5.5 유지 (최적 6.5~7.5)
- BOD 제거율 85% → 60% 하락
- 방류수 기준 근접 (경고)
해결:
- 유입수 pH 모니터링 강화
- RSWT 투입량 자동 조절 시스템 도입
- pH 6.5 미만 시 알람 설정
pH 관리는 폐수처리의 알파이자 오메가
폐수처리에서 pH는 단순한 측정값이 아닙니다. 생명과 죽음, 성공과 실패를 가르는 절대 척도입니다.
pH가 최적 범위(6.5~7.5)를 벗어나면:
- ❌ 미생물이 죽습니다
- ❌ 화학 반응이 멈춥니다
- ❌ 설비가 부식됩니다
- ❌ 법규를 위반합니다
- ❌ 수천만 원의 손실이 발생합니다
반대로 pH를 안정적으로 관리하면:
- ✅ 생물학적 처리 효율 95% 이상
- ✅ 중금속·인 제거 최적화
- ✅ 설비 수명 2~3배 연장
- ✅ 약품비 30~40% 절감
- ✅ 법규 완벽 준수
- ✅ 기업 신뢰도 향상
RSWT의 완충 시스템은 이 모든 것을 가능하게 하는 혁신입니다.
기존 소석회 방식의 "pH 스파이크" 문제를 근본적으로 해결하고, 자동 중화·안정화·완충의 3박자를 완벽히 구현합니다.
pH 관리는 폐수처리의 시작이자 끝입니다.
오늘부터 pH를 과학적으로, 체계적으로, 안정적으로 관리하십시오.
'폐수처리 산업 동향 & ESG 경영' 카테고리의 다른 글
| 섬유·염색 산업의 산성 폐수 중화에 RSWT를 활용하는 사례 (0) | 2026.04.01 |
|---|---|
| 산업폐수 재이용, 경제성 분석 (0) | 2025.12.31 |
| 순환경제 시대, 폐기물을 자원으로 바꾸는 기술 (0) | 2025.12.30 |
| 제조업체가 놓치기 쉬운 폐수처리 법규 (0) | 2025.12.30 |
| 폐수처리 설비 개선, ROI 계산하는 법 (0) | 2025.12.29 |
